プロローグ
あれは1974年3月の末だったろうか。東京駅八重洲口の地下食堂で、筆者は、同門で5年ほど後輩になる野本明男さんと飯田滋さんの3人と酒を酌み交わした。この日、野本さんの同期の人達の博士号取得のお祝いが研究室であって上京し、その帰りだった。筆者は4年前から国立遺伝学研究所へ勤めていたので、二人は、新幹線の最終便で三島へ帰る私を送ってきてくれたのだ。この飲み会はまた、2~3か月以内に3人がそれぞれ海外へ留学することになっていたので、自然に、3人だけの壮行会にもなっていた。恩師の浮田忠之進教授(東大薬・衛生裁判学)が2年前に亡くなられていたので、就職先など将来のことに関して、皆が不安な中に居た。若い二人は、豪気なところがあって、「なに、海外で良い仕事をして認められれば、何とかなるさ」ということであった。「いい仕事をして帰ってきても、先生がいなければ、就職先を世話してくれる人がいないかもしれない」などという一抹の不安もあることだったが、それを振り切るように、これから留学先でやると思われる研究について3人の話は弾んだ。
飯田さんは、スイス・バーゼルにあるBiozentramのArber(Werner Arber)研究室へ行き、DNAを切断する制限酵素の研究をするという。制限酵素は、飯田さんが、学生時代から言い続けていた「やりたい研究である」。一方、野本さんは、米国ニューヨーク州ロングアイランドにあるニューヨーク大学StonyBrook校のWimmer(Eckard Wimmer)研究室へ行き、ポリオウイルスの研究をやるという。「えっ、ウイルスやるの、大丈夫? 今まで核酸の化学しかやってないのに、ポリオウイルスできるの?」。「そんなこと言ったって、古市さんだって、tRNAしかやってなかったのに、いまはウイルス屋さんじゃないですか」ーーと、こんな、話が続いたーー。筆者は、野本さんに「ポリオウイルスのRNAはプラス鎖だから、メッセンジャーRNAと同じなので、CPVウイルスのように5′末端はメチル化され、ブロック構造になっていると思うから、それをまずそれをWimmer研でやってみたら」と勧めた。
「僕が行くニュージャージー州のロシュ分子生物学研究所は、ロングアイランドのNY大へは、車で4時間くらいで行けるから、実験のコーチに行ってやるよ」ということで、最後は、お互いに心強い会話で盛り上がって別れた。
さて、こんな壮行会で別れた3人だったが、その後、飯田さんはスイスに20年以上、筆者は米国に10年以上残って研究を続けることになるから「ーー先のことは全く判らない」。野本さんは、2年後、ポリオウイルスの研究を持ち帰り、遺伝子工学を駆使して師匠のWimmerも及ばぬ良い研究をすることになる。この稿では、ポリオウイルスで時代の先端をひらいた若い日の野本さんの仕事からスタートして、前の項で述べたキャップ結合タンパクeIF4Eの働きをダメにするポリオウイルス(あるいは、ノロウイルス)の悪辣な戦略と、そこから発して発見されたキャップ非依存的なmRNAの翻訳メカニズムや、IRESの発見について紹介したい。
すべては、ポリオRNAから始まった
ポリオウイルスは小さなRNAウイルスである。ウイルス粒子の中に、一本の、プラス鎖(つまりmRNAとおなじ)一本鎖(ss)RNAがゲノムとして入っている。ウイルスの分類では、ピコルナ科(ピコ=小さい、ルナ=RNA)に属し、最近、感染件数が増えているノロウイルスも同様のウイルスである。これらのウイルスは、腸管細胞に感染し、発熱や下痢・嘔吐などの消化器症状の原因となる。ポリオウイルスは、小児の足に麻痺を引き起こすウイルスとして恐れられてきたことから、ワクチン開発の歴史も長く、最もよく研究されたウイルスであった。一時代前の研究では花形であった大腸菌に感染するRNAファージに似たところがあり、HeLa 細胞での増殖も確立しており、有核細胞に感染するウイルスのさきがけ的なウイルスとなっていた。小児麻痺の原因としては、腸管で増えたウイルスの一部が血流へ入り、この中から筋肉の神経細胞へ感染したり、変異したウイルスが稀に血液脳関門(Brain-Blood barrier)を通過して脳へ侵入したり、さらに稀に、脳内の神経細胞中で増殖できる変異ウイルスが出現して、脳神経の一部の細胞が侵される病状がでる。そのため、ウイルス側の変異に関する研究と、ウイルスと宿主細胞の関係を調べる研究が焦点になっていて、野本さんの興味もこれらの点にあった。ポリオウイルスの米国での研究は、私のみるところMITのDavid BaltimoreとWimmerの二つのグループがあり、競い合っていたが、この時点でBaltimoreの声は大きかった(もともと地声の大きい人であるが、1975年、逆転写酵素の発見でノーベル賞を取ってから一層大きくなったような気がする)。ポリオウイルスのゲノムRNA(mRNAと同じ配列を持つ)は、7700塩基ほどであり、長い一本のタンパク質を作るのに使われ、そのタンパク中コードされるプロテアーゼが長いタンパクを(自己裁断して)正確に切り分けて、約10種のウイルスタンパク質を作る。余談になるが、後年、野本さんに入れ替わってWimmer研へ留学した同門の喜多村直美さんによって、ゲノムRNAの全配列が決定されている44。
さて、野本さんはWimmer研に入所後、ただちにポリオRNAの5′末端について調べ始めた。新しいポスドクが来るときには、ボスはあらかじめテーマを決めておくのであるが、我々2人が東京駅で話したテーマには、Wimmer先生も賛成したらしい。そのころ、筆者もShatkin研へ入所し、第一話で書いたような忙しさで、レオウイルスのmRNAを手始めに、アデノウイルス、レトロウイルスやHeLaの細胞mRNAやHnRNAなど手広く各種RNAの5′末端にあるキャップ構造を発表していたし、他の研究室からも論文は続々出ていた。野本さんとは、電話で実験方法などについて細かく相談していたが、HeLa細胞中から取れるポリオウイルスmRNAにはキャップは見つからなかった。最終的には、全体を強烈に32Pで標識したポリオウイルスmRNAを作り、ポリAカラムで精製し、リボヌクレアーゼT2で分解して5′末端に由来するヌクレオチドを調べると、5′末端はpUpであることがわかった。つまり、渡米前に、東京駅の食堂で予想していた「メチル化されていてブロック構造を持つキャップ構造」はポリオにはなかったのである。この時期、次々とキャップの存在とその物語が広がって行く中で、ポリオウイルスのmRNAにはキャップがないという発見は、むしろこの時期、快挙であった。そして「RNA World」を一層複雑に、かつ面白くしてくれることになり、野本さんのこのポリオmRNAの仕事は論文になり、PNAS誌上で発表された。そのタイトルが面白い。"The 5′ end of poliovirus mRNA is not capped with m7GpppNp" (Nomoto, Lee & Wimmer45)である。このタイトルには、少々驚いたが、ドイツ人エッカードWimmerの反骨精神が顕れていて、私は好きだ。
その後、ウイルス粒子から抽出したポリオゲノムRNAには、pUpの先にVpgという小さなタンパクが共有結合で付いていることをLee, Nomoto, Wimmerの3人の実験から見出した。すでにアデノウイルスのゲノムDNAにタンパク質がついていることは知られていたが、RNAの末端にタンパク質がついていることは新発見であった。エッカードによると、この実験は、自分が手を下した最後の実験なので、思い出が深い、とのことである。
あまた多くのウイルスゲノムやmRNAではキャップがついている中で、Vpg-RNAは異色であった。そして、野本さんには2報目のPNAS論文が出て、ポリオRNAの5′末端に決着がついた。そのタイトルは、"A protein covalently linked to poliovirus genome RNA" (Lee, Nomoto, Detjen & Wimmer46) であり、これは、東京駅発の研究のエキサイティングなエンディングだった。
タンパク質(Vpg)がリードする奇妙なRNA合成
その後、Wimmer研やBaltimore研の研究から、ポリオウイルスをはじめとするピコルナ科のウイルスのRNA合成では、ウイルスのRNAポリメラーゼの一部であるVpgタンパク(――ポリオウイルスの場合22アミノ酸よりなるぺプチドーー)がプライマーとして働かねば進まないことが判った。ただし、Vpgは単独で働くのではない。Vpg中にあるチロシン残基のOH基に、細胞中のUTPが反応し、Vpgをウリジル化する奇妙な反応が起こり、そこで生じるVpg-pUやVpG-pUpU-がピコルナ科のウイルスの複製や転写の際にプライマーとしてはたらくのである。野本さんの発見になるpUP-mRNAは、じつはVpg-Tyr-pUU-RNAが、細胞内の酵素によってVpgが外されたRNAであったと思われる。このポリオウイルスRNAの発見から、野本さんを筆頭著者とするPNASとNature論文が発表された47,48。そこでは、本来ポリメラーゼの一部であるVpgが「RNA合成のスターターとしてはたらくのではないか」という仮説を提唱しているが、筆者はこれに大賛成である。
さて、これらのRNA上の発見は、ポリオウイルスのmRNAがキャップによらない他の方式でタンパク合成を行っていることを暗に示すものであり、タンパク合成に関わる研究者にとっては、魅力的な謎を残すこととなった。加えて、RNAの5′末端に結合した小さなVpgタンパクの役割についても、RNAゲノムの複製にも必要であることがわかり、それはそれで、新しい研究分野を拓くことになった49。当然だが、エッカードの声は、ポリオウイルスに関しては、デビッドBaltimoreに負けず大きくなっていた。
その後、同様のVpgは、他のピコルナウイルスや、鼻かぜの原因として知られるライノウイルスにも存在することが判るのであるが、きまってVpgのうしろにはtRNAに似たクローバー型の2次構造があり、そのまた後ろにはーーキャップなしでリボソームを引き寄せるーーIRES配列(このあと紹介)が続くことが発見された(図1)。
筆者などは、“風邪をひいたかな”と思うとき、ハテ、この症状はキャップを盗むインフルエンザ型(第4話で紹介した)かな、あるいは、キャップを必要としないポリオウイルス型かなどと、ついつい、ウイルスの生化学へ思いを馳せるのである。
<脱線ご容赦> この頃、筆者は家族が一時的に帰国していたこともあって、野本さんやエッカードを訪ねて、泊りがけでよくStonyBrookへ出かけた。そこでは、日本語で話ができるという楽しみがありーー、ニューヨーク大(StonyBrook校)に研究室を構えていられた井上正順先生夫妻、大坪栄一夫妻ともお会いして話ができるので、実家へ戻った感があり、釣り、ゴルフ、夜っぴてのカードゲームを楽しんだ。
大学の隣町には、ポートジェファーソンという古い港町がある。港は、対岸のコネチカットへ船が出ていて、船着き場の正面に魚屋があり、ここで茹でて出してくれるチムニーという貝が美味しくて、必ず立ち寄った。酒類も出してくれるので。ハマグリ大の貝から、オチンコが出ているように突き出ているチムニー(煙突の意味だろう)部分をつまんで、貝から放し、溶けたバターにシャブシャブ浸して食べるのであるが、これが実に美味しい。貝の薄い塩味とバターがからんで、いい味を作る。大ぶりのグラスの縁に少しばかり塩をのせた冷たいマルガリータや、冷たいビールでチムニーをつまむのは最高だった。私とエッカードはテニスをやるので、時折、二人だけでシングルスゲームを楽しんだ。彼の左利きのストロークやサーブは食い込んでくる“くせ玉”なので、これを打ち返すのが実に難しい。まるでキャップやキャップ結合タンパクが、それと対抗するポリオウイルスを相手に戦うような気がしたものである。
ポリオウイルスのタンパク合成
ポリオウイルスに感染した細胞では、急速に、タンパク合成ができなくなってしまうという現象がある。
この現象はシャットオフ(shutoff)と呼ばれていて、そんな状態の細胞のmRNAを調べてみると、キャップを持ったmRNAは健全であるにもかかわらず、リボソームへ結合できなくなっていることがわかった。つまり、キャプ依存型のタンパク合成が、何故か、ウイルス感染後、出来なくなってしまうのである。一方、キャップを持たないポリオウイルスのmRNAやEMCウイルス(encephalomyocarditis virus)のmRNAは、そのような細胞中で、順調にリボソームへ結合し(――あるいは、“リボソームに結合されて”)無事に、複製に必要なタンパク質を作るのである。
たとえ話にすると、この状況はーーポリオウイルスが宿主細胞のタンパク合成工場へ侵入し、工場のシステムを乗っ取り、キャップを使う作業手順書を破り捨て、キャップを使わない方式の作業手順書にすり替える、というようなことである。工場の機器や装置は温存し、壊さないで、なるべくそのままで使うのである。そうすれば、キャップを持たない自分のmRNAを使ってタンパクが作れるのである。このメカニズムは、その後、WimmerやBaltimoreのグループ、それにキャップ結合タンパク発見者のナフムSonenbergのグループにより、次々に解明された。
すなわち、ポリオウイルスが作るプロテアーゼ(2A)が、宿主のeIF4E(キャップ結合タンパク)を載せる土台ともいうべきeIF4F(あるいはeIF3)中のp220というタンパク質にカットを入れて壊してしまい、eIF4EがmRNAのキャップに結合できなくすることが、シャットオフの一つの理由であることが判った50。すなわち、第6話で紹介した、クロスリンクの方法では、もはやキャップを持つ宿主細胞のmRNAは、eIF4Eにクロスリンクしなくなるのである51。そのうえで、ポリオウイルスは、5′末端から500塩基ほど入ったところにあるIRES(図1で紹介)と呼ばれる特定の構造中の開始コドンへリボソームを誘導してタンパク合成を始動する52,53。IRESはInternal Ribosome Entry Siteの略であり、特殊な2次構造で作られていて、長いmRNA鎖の中に一か所しかないことが判った。したがって、作られるタンパク質はポリプロテインと呼ばれる長いタンパク質であり、それがプロテアーゼによって切断された10種類ほどの数のタンパク質が作られる。先に述べたVpgはそのうちの一つであり、RNAポリメラーゼの一部でもある。
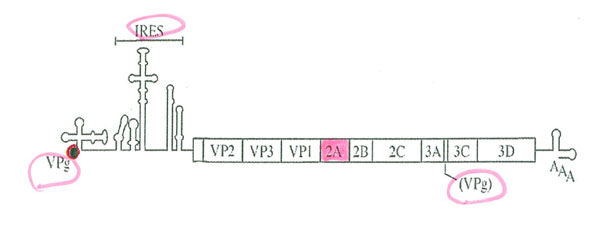
図1:ポリオウイルスのRNA
ポリオウイルスの、このような感染戦略はシンプルで効率が良い。一方、長期にわたる感染後に、ヒトに肝癌を頻発するC型肝炎ウイルスも、これらのポリオウイルスの研究から、同様に、IRESを使った戦略でタンパク合成を行うことが判ってきた。これらのタンパク合成の方法は、原始的なRNAウイルス(ファージ)にその面影が偲ばれるのであり、ウイルスの進化を考えるとき、ウイルスのmRNAがキャップ依存型かIRES依存型なのかの観点から比較するのは興味深い。
Wimmer研における日本人研究者の多大な貢献
エッカードは、ラッキーな男だと思う。1970年代から優れた日本人研究者が次々とポスドクとして研究室へ入り、独立したばかりのエッカードの重要な時期に、数々の良い成果を積み上げて貢献した。その最初は、ポリオウイルスRNAの3′末端にポリAを証明した余郷嘉明さん(後に東大医科研教授)だろうか。筆者は、余郷さんとは研究室は違うが東大薬大学院で同期だ。その後に、この稿で紹介した野本明男さん(後に東大医教授)がWimmer研へ入り、RNAの5′末端の問題を解いた。その後を引き継いで、同門の喜多村直美さん(後に東工大教授)が続き、ポリオウイルスRNAの全配列を決定するなど、Wimmer研の初期の代表的な研究は、全て東大薬出身の日本人研究者の活躍に負っている。
一昨年、野本さんの追悼シンポジュームが東京都臨床研で行われた際、筆者も招かれて、エッカードと三十数年ぶりに再会を果すことが出来た。彼は私より5歳年上であり、今年は80歳だが、まだ元気でNY大の有名教授として現役であるという。講演の中でも言っていたが、「私のこれまでの研究と現在があるのは、日本人研究者のお陰である」と素直にお礼を言っていたのには、お世辞ではないことを知る筆者には、真に嬉しかった。「自分がまだ現役でいる間にNY大へ来て、話題はなんでもいいから、講演してくれ」という嬉しい誘いを受けているが、そのうち出かけて行って、講演後、ポートジェファーソンでチムニーとマルガリータを楽しみたいと思っている。
この稿を書くにあたり、エッカードへ昔の研究室の様子を写した写真を提供してくれることを頼んだのだが、まだ送られてこないところをみると、見当たらないらしい。替わりにと言ってはなんだが、野本さんを偲んで、彼の3回忌に、さきがけRNA塾の皆さんと一緒に富士霊園にある野本さんのお墓へ詣でたので、その折の写真を載せたいーー好天で、富士山が映える良い日だった。

図2:野本さんを偲んで
エピローグ
この稿を東京駅での飲み会から始めたが、同席した飯田滋さんは永くバーゼルのBiozentrum研究所でウエルナーArber先生とトランスポゾンやバクテリオファージを用いて、DNA構造と組み換え現象の研究を続けていた。1978年10月のある日、ストラスブルグで開かれた国際ウイルス学会へ出席した筆者は、帰りにバーゼルへ飯田さんを訪ねた。Arber研究室は、米国の研究室に比べると、小所帯で、静かな雰囲気であり、「腰を落ち着けて、飯田さんの好きなDNA dynamicsの研究ができるだろう」という感想をもった。DNA組み換えに関する研究は、筆者には、難しくてよくわからなかったが、Arber先生と飯田君は、時間をかけて、丁寧に研究の中身を紹介してくれた。翌日、研究所のセミナー会での講演を無事終えて、筆者は二人と別れてマッターホルンを見るために、汽車でツェルマット村へ向かった。この山行きの計画を話した時、Arber先生は「僕も、明日から山へ行く。天気は良さそうだから、我々はラッキーだ。アルプスが綺麗に見えるはず」と言ってくださった。ーーその日は、金曜日だったのかもしれない、マッターホルンを見てから、その翌日、米国のJFK空港に降り立った。空港で、NYタイムズ誌を買ったところ、その前日に、ノーベル医学・生理学賞が、制限酵素の発見に関して、Arber先生を含む3人の研究者に与えられることが報じられているのを見て、ビックリした。「ああ、もう一日、Arber研にいたら、一緒にお祝いできたのにーー残念!」。「いや待てよ、Arber先生は山へ行くと言っていたから、このニュースはまだ先生へ伝わってなくて、独り留守を預かった飯田君は、先生がいなくて、“てんてこ舞い”をしているのではなかろうか」と案じたものであるーー後日、飯田さんから聞くところによると、やはりそのようだったらしい。
研究稼業は元来静かなものであるが、時折、神様はこのような茶目っ気をなさる。ボスがノーベル賞を取るようであれば、飯田君が続けたかった研究の行く末は「安泰であろう」と感じた。――そんなことで、東京駅で別れた3人には、それぞれに、エキサイティングな場面があったのだが、それらを良き想い出として、大切にしている。
(了)
< 第一回 | 第二回 | 第三回 | 第四回 | 第五回 | 第六回 | 第七回 | 第八回 | 第九回 | 第十回 | 第十一回 | 第十二回 | >
References
1. Miura K, Watanabe K, Sugiura M, Shatkin AJ.
The 5′-terminal nucleotide sequences of the double-stranded RNA of human reovirus.
Proc Natl Acad Sci U S A. 1974 Oct;71(10):3979-3983.
PMID: 4530278
2. Furuichi Y.
"Methylation-coupled" transcription by virus-associated transcriptase of cytoplasmic polyhedrosis virus containing double-stranded RNA.
Nucleic Acids Res. 1974 Jun;1(6):809-822.
PMID: 10793759
3. Smith AE.
Modified nucleotides in messenger RNA?
Nature 1974 Aug;9 250(5466) 461.
PDF (237K)
4. Furuichi Y, Miura KI.
Identity of the 3′-terminal sequences in ten genome segments of silkworm cytoplasmic polyhedrosis virus.
Virology. 1973 Oct;55(2):418-425.
PMID: 4742779
5. Furuichi Y.
Discovery of m(7)G-cap in eukaryotic mRNAs.
Proc Jpn Acad Ser B Phys Biol Sci. 2015;91(8):394-409.
PMID: 26460318
6. Furuichi Y, Miura K.
A blocked structure at the 5′ terminus of mRNA from cytoplasmic polyhedrosis virus.
Nature. 1975 Jan 31;253(5490):374-375.
PMID: 163011
PDF (414K)
7. Furuichi Y, Morgan M, Muthukrishnan S, Shatkin AJ.
Reovirus messenger RNA contains a methylated, blocked 5′-terminal structure: m-7G(5′)ppp(5′)G-MpCp-.
Proc Natl Acad Sci U S A. 1975 Jan;72(1):362-366.
PMID: 1054511
8. Wei CM, Moss B.
Methylated nucleotides block 5'-terminus of vaccinia virus messenger RNA.
Proc Natl Acad Sci U S A. 1975 Jan;72(1):318-322.
PMID: 164018
9. Adams JM, Cory S.
Modified nucleosides and bizarre 5'-termini in mouse myeloma mRNA.
Nature. 1975 May 1;255(5503):28-33.
PMID: 1128665
PDF (1.6M)
10. J. Darnell H. Lodish D. Baltimore
Molecular Cell Biology
Scientific American Books, W. H. Freeman and Company. (1986)
11. James E. Darnell.
RNA: Life's Indispensable Molecule
Cold Spring Harbor Laboratory Press. ISBN: 978-1-936113-19-4.
CSH Press
Amazon.co.jp
12. Furuichi Y, Morgan M, Shatkin AJ, Jelinek W, Salditt-Georgieff M, Darnell JE.
Proc Natl Acad Sci U S A. (1975) 72(5):1904-1908.
PMID: 1057180
13. Furuichi Y, Muthukrishnan S, Tomasz J, Shatkin AJ.
J Biol Chem. (1976) 251(16):5043-5053.
PMID: 821947
14. Abraham G, Rhodes DP, Banerjee AK.
Cell. (1975) 5(1):51-58.
PMID: 165900
15. 古市 泰宏
蛋白質・核酸・酵素 (1977) 22(10), 1201-1204.
16. Sommer S, Salditt-Georgieff M, Bachenheimer S, Darnell JE, Furuichi Y, Morgan M, Shatkin AJ.
Nucleic Acids Res. 1976 Mar;3(3):749-765.
PMID: 1272797
17. Amiya K. Banerjee
Proc Natl Acad Sci U S A. (2012) 109(46):18629-18630.
18. Furuichi Y, Shatkin AJ, Stavnezer E, Bishop JM.
Nature. 1975 Oct 16;257(5527):618-620.
PMID: 170541 PDF
19. Gelinas RE, Roberts RJ.
Cell. 1977 Jul;11(3):533-544.
PMID: 884734
20. Thomas M, White RL, Davis RW.
Proc Natl Acad Sci U S A. 1976 Jul;73(7):2294-2298.
PMID: 781674
21. Berget SM, Moore C, Sharp PA.
Proc Natl Acad Sci U S A. 1977 Aug;74(8):3171-3175.
PMID: 269380
22. Krug RM, Morgan MA, Shatkin AJ.
J Virol. 1976 Oct;20(1):45-53.
PMID: 1086370
23. Plotch SJ, Krug RM.
J Virol. 1977 Jan;21(1):24-34.
PMID: 833924
24. Bouloy M, Plotch SJ, Krug RM.
Proc Natl Acad Sci U S A. 1978 Oct;75(10):4886-90.
PMID: 283399
25. Furuichi Y, Shatkin AJ.
Proc Natl Acad Sci U S A. 1976 Oct;73(10):3448-52.
PMID: 185613
26. Bouloy M, Morgan MA, Shatkin AJ, Krug RM.
J Virol. 1979 Dec;32(3):895-904.
PMID: 513205
27. Furuichi Y.
Review:Caps on Eukaryotic mRNAs. In: eLS. John Wiley & Sons, Ltd: Chichester.
DOI: 10.1002/9780470015902.a0000891.pub3
28. Krug R.M. and Fodor E.
Webster-Textbook of Influenza
Wiley
Amazon
29. Urushibara T, Furuichi Y, Nishimura C, Miura K.
FEBS Lett. 1975 Jan 1;49(3):385-9.
PMID: 162886
30. Shatkin AJ.
Proc Natl Acad Sci U S A. 1974 Aug;71(8):3204-7.
PMID: 4528644
31. Hickey ED, Weber LA, Baglioni C.
Nature. 1976 May 6;261(5555):71-2.
PMID: 944859
32. Enigma Variations’ of mammalian messenger RNA. (News & Views)
Nature. 1975 May 1;255(5503):9
PDF
33. Muthukrishnan S, Both GW, Furuichi Y, Shatkin AJ.
Nature. 1975 May 1;255(5503):33-7.
PMID: 165427
34. Both GW, Banerjee AK, Shatkin AJ.
Proc Natl Acad Sci U S A. 1975 Mar;72(3):1189-93.
PMID: 165487
35. Both GW, Furuichi Y, Muthukrishnan S, Shatkin AJ.
Cell. 1975 Oct;6(2):185-95.
PMID: 1182800
36. Furuichi Y.
Proc Natl Acad Sci U S A. 1978 Mar;75(3):1086-90.
PMID: 349555
37. Furuichi Y, LaFiandra A, Shatkin AJ.
Nature. 1977 Mar 17;266(5599):235-9.
PMID: 557727
38. Filipowicz W, Furuichi Y, Sierra JM, Muthukrishnan S, Shatkin AJ, Ochoa S.
Proc Natl Acad Sci U S A. 1976 May;73(5):1559-63.
PMID: 1064023
39. Sonenberg N, Shatkin AJ.
Proc Natl Acad Sci U S A. 1977 Oct;74(10):4288-92.
PMID: 270673
40. Sonenberg N, Morgan MA, Merrick WC, Shatkin AJ.
Proc Natl Acad Sci U S A. 1978 Oct;75(10):4843-7.
PMID: 217002
41. Nahum Sonenberg
Biochem Cell Biol. 2008 Apr;86(2):178-83. doi: 10.1139/O08-034.
PMID: 18443631
42. Lazaris-Karatzas A, Montine K.S. Sonenberg N.
Nature. 1990 Jun 7;345(6275):544-7.
PMID: 2348862
43. Lazaris-Karatzas A. Sonenberg N.
Mol Cell Biol. 1992 Mar;12(3):1234-8.
PMID: 1532049
44. Kitamura N, Semler BL, Rothberg PG, Larsen GR, Adler CJ, Dorner AJ, Emini EA, Hanecak R, Lee JJ, van der Werf S, Anderson CW, Wimmer E..
Nature. 1981 Jun 18;291(5816):547-53.
PMID: 6264310
45. Nomoto A, Lee YF, Wimmer E.
Proc Natl Acad Sci U S A. 1976 Feb;73(2):375-80.
PMID: 174106
46. Lee YF, Nomoto A, Detjen BM, Wimmer E.
Proc Natl Acad Sci U S A. 1977 Jan;74(1):59-63.
PMID: 189316
47. Nomoto A, Kitamura N, Golini F, Wimmer E.
Proc Natl Acad Sci U S A. 1977 Dec;74(12):5345-9.
PMID: 202952
48. Nomoto A, Detjen B, Pozzatti R, Wimmer E.
Nature. 1977 Jul 21;268(5617):208-13.
PMID: 196204
49. Wimmer E.
Cell. 1982 Feb;28(2):199-201.
PMID: 7060125
50. Etchison D, Milburn SC, Edery I, Sonenberg N, Hershey JW.
J Biol Chem. 1982 Dec 25;257(24):14806-10.
PMID: 6294080
51. Kräusslich HG, Nicklin MJ, Toyoda H, Etchison D, Wimmer E.
J Virol. 1987 Sep;61(9):2711-8.
PMID: 3039165
52. Lee KA, Sonenberg N.
Proc Natl Acad Sci U S A. 1982 Jun;79(11):3447-51.
PMID: 6954488
53. Sonenberg N, Pelletier J.
Bioessays. 1989 Nov;11(5):128-32.
PMID: 2556117






